кристална структура
ГЛАВА I. структурата и свойствата на метали
§ 1. кристална структура
Видове кристални решетки. Твърдите вещества се разделят на кристални и аморфни. Кристална тяло по време на нагряването остане твърдо вещество до определена температура (температура на топене), при което те преминават в течно състояние. Аморфен тяло омекотена чрез нагряване в голям температурен диапазон; Първо те сгъстят и едва след това се втечни.
Всички метали и техните сплави - кристални твърди вещества. Метали, наречени химични елементи, които са характерните черти на непрозрачността, гланц, добра електрическа и топлинна проводимост, еластичността и за много метали способността да се заварява. Това не е загубил своята решителност научна стойност на метали, преди това повече от 200 години от големия български учен М. В. Lomonosovym: "Метали са светлината на тялото, които могат да се изградят." За метали, характеризиращ се с това, че чрез въвеждане в химична реакция с елементите, които са неметали, те дават последната си външен, валентните електрони. Това се дължи на факта, че металните атоми хлабаво свързани външните електрони от ядрото. Метали са на външната обвивка само 1-2 електрон, докато много неметали такива електрони (5-8).
Чисти химически елементи на метали (например, желязо, мед, алуминий и т.н.) могат да образуват комплекс вещество, чийто състав може да включва няколко метални елементи, често с примеси елементи, значителни количества от неметали. Такива вещества са посочени като метални сплави. Прости вещества, формиращи сплав, наречена Лети компоненти.
За да се опише кристалната структура на метали използва концепция решетка. Кристалната решетка - въображаема пространствена решетка, възлите, които са разположени атоми (йони), представляваща металът. Вещество частици (йони, атоми), от които се изграждат кристал, разположени в определен геометричен модел, който се повтаря периодично в пространството. За разлика от кристали в аморфни структури (стъкло, пластмаси) атоми са разположени в пространството на случаен принцип, на случаен принцип.
Образуването на кристалната решетка на метала, както следва. Когато металът преминава от течност към твърдо състояние, разстоянието между атоми се намалява и силата на взаимодействие между тях се увеличава. взаимодействия символи атома определят от структурата на техните външни електронни черупки. При приближаване атома електрони, разположени на външните мембрани, те губят контакт с техните атоми поради отделяне на валентност електрон на атом положително заредена ядро на друга и така нататък. Е. образуването на свободни електрони, тъй като те не принадлежат към един атом. Така в състояние метал твърдо вещество е структура, състояща се от положително заредени йони, промиват свободни електрони.
Комуникация в метала се извършва от електростатични сили. Между йони и свободни електрони възникне електростатично привличане сили, които стягат йони. Такава връзка между металните частици, наречени метал.
Свързващите сили в метали се определят от сили на отблъскване и сили на привличане между йони и електрони. Йоните са разположени на разстояние един от друг, в които потенциалната енергия на взаимодействие е минимална. метални йони са разположени в определен ред, за да образуват решетка. Тази конструкция се осигурява от взаимодействие на йони с техните валентните електрони, които се свързват йони в кристалната решетка.
Видове кристални решетки в различни метали. Най-често решетката: тяло центрирана кубична (Ск), лице центрирана кубична (FCC) и шестоъгълна плътно опаковани (НСР). Най-малкият размер на кристала, дава представа за атомна структура на метала в някоя от обема си, наречен елементарен кристален клетка (фиг. 1). Тя се характеризира с кристалната решетка параметри като дължина куб ръбове за Ск и FCC, което прави за различни метали -8 2.8610 cm.
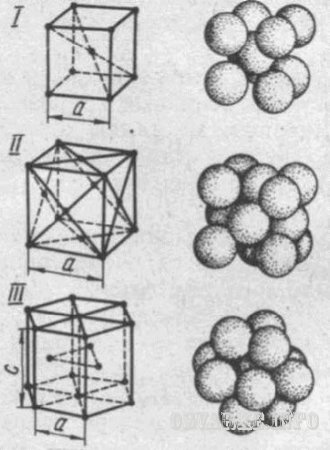
Фиг.1. Клетките единични кристални решетки:
I - обем центрирана кубична (-iron), II - лице центрирана кубична (мед); III - хепатит; и и - параметрите на решетки
Дефекти в кристали. В кристалите, винаги има дефекти (несъвършенства) структура, причинени от смущения на правилното позициониране на кристалната решетка на атома. Дефекти в кристалната структура са разделени от геометричните характеристики на точка, линия и повърхност.
Атомите осцилира до точките на решетка и температурата се увеличава амплитудата на тези вибрации се увеличава. По-голямата част от атомите на кристалната решетка има същото (средно) енергия диапазона и за дадена температура със същата амплитуда. Въпреки това, отделните атоми имат енергия значително по-висока средна енергия и се премества от едно място на друго. Най-лесно да се движат атомите на повърхностния слой, оставяйки повърхността. А мястото, където е налице такава атом се нарича свободно място (фиг. 2а). На това място след известно време се движат един от атомите на съседния слой и отворено положение така нататък. Е. така се движи във вътрешността на кристала. С увеличаване на температурата, броят на свободните работни места се увеличава и те са по-склонни да се преместят от един възел към друг. Процесите на дифузия в метали, работни места, играят решаваща роля. Към недостатъците на точките са също атом, интерстициален решетка (фиг. 2Ь), и заместен атом, когато на мястото на един от метален атом в решетката е заменен от друг, чужд атом. Point дефекти предизвика локално нарушаване на кристалната решетка.
Линейни дефекти са изгледи на други съществени недостатъци на кристалната решетка в резултат на срязване на една interatomic разстояние на една част от решетка спрямо друго по продължение на равнината брой редове атоми в решетката на горната част на един по-голям, отколкото на дъното. В този случай няма да има допълнително като атомен самолет в горната част на решетката (допълнителните). Ръбът допълнителните перпендикулярна на посоката на плъзгане, се нарича ръб или линеен дислокация (фиг. 2с), продължителността на който може да достигне много хиляди interatomic разстояния. Wide разгръщане е разстоянието от центъра на мястото на решетка дефект без изкривяване. ширина дислокация е малък и е в размер на няколко атомни разстояния.
Кристалната решетка размествания в зоната еластично деформирани, от атомите в тази зона се изместват по отношение на тяхната равновесно състояние. За размествания характеризират с лесно тяхната мобилност. Това се дължи на факта, че атомите, образуващи дислокацията има тенденция да се движат в равновесно състояние. На размествания са образувани по време на кристализацията на метали (вж. Chap. 1, § 2), както и пластична деформация, топлинна обработка и други процеси.
Повърхностни дефекти са интерфейси между отделните кристали (Фиг. 2D). В интерфейса между атомите на кристала са по-добре, отколкото в по-голямата част. В допълнение, интерфейсите натрупват изкълчвания и места, както и концентрирани примеси, които допълнително нарушава реда на подреждането на атомите. Освен това, тези кристали се misoriented, т. Е. Може да се завърта спрямо друга от десетки градуса. съдържание на метал може да се увеличи поради нарушаване на кристалната решетка близо до границите или намалението поради наличието на примеси и концентрация дефект. Дефектите в кристалите значително влияят на метални свойства.
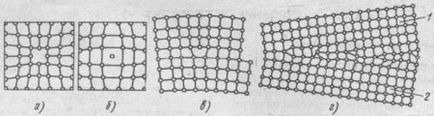
Фиг. 2. Дефекти в кристалите:
и - отворено положение, б - жива атом в - линеен ръб дислокация г - неправилна атома NNA зърно граница 1 и 2
Анизотропия кристали. Разлики от физичните свойства на средата, в различни посоки се нарича анизотропия. Анизотропия на кристала, причинено от разликата в опаковане плътност на атома в решетката в различни посоки. Всички кристали са анизотропни и аморфни вещества (стъкло, смола) са изотропни, т.е.. Е. Има същия атом плътност в различни посоки.
На анизотропия на свойства е важно при използване на единични кристали - единични кристални частици, които са разположени равномерно в обема им. Единични кристали имат редовен кристал аспект (под формата на природен polyhedra) са анизотропни в механични, електрически и други физични свойства. По този начин, за якост на опън на единичен кристал меден # 963; в се променя 120-360 МРа, в зависимост от посоката на прилагане на натоварването.
Метали и сплави, използвани в областта, обикновено имат структура поликристален. т. е. да се състои от множество малки и различно ориентирани кристали не с нормална кристал нарязани и наречени кристалити (или зърна). Всеки зърно Поликристалната наблюдава анизотропия. Въпреки това, поради различни, произволно кристалографски ориентация самолети различни зърна Поликристалната могат да имат същите свойства в различни посоки и не откриват анизотропия (когато размерът на зърното е много по-малък от размера на Поликристалната и броят им е много голям). Това обстоятелство в много случаи може да се разглежда като изотропно поликристален тяло въпреки анизотропни свойства на отделните съставни зърната.
Печелете по тяхно знание. Отговорете на въпросите и да се плаща за това!