Ковалентното химични връзки - е
дефиниция
Ковалентна връзка се нарича химична връзка се формира поради социализацията на техните атоми на валентните електрони. Предпоставка е образуването на припокриване ковалентна връзка на атомна орбитална (AO), които са разположени валентните електрони. В най-простия случай, две припокриващи AB води до образуването на два молекулно орбитален (МО) свързване на МО и antibonding (antibonding) MO. Споделени електрони, разположени на по-ниска свързваща енергия MO:
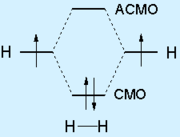
лепене
Ковалентна връзка (атомна връзка, ковалентна връзка) - връзка между два атома поради социализация (електрон споделяне) два електрона - един от всеки атом:
Поради тази причина, ковалентна връзка е посока. Една двойка електрони в комуникация принадлежи едновременно двете свързващи атоми, например:
Видове ковалентна връзка
Има три вида ковалентна химическа връзка, различна от механизма на неговото формиране:
1. единична ковалентна връзка. За неговото формиране всеки атом осигурява една несдвоен електрон. При образуването на единична ковалентна връзка официални такси на атомите остават непроменени. Ако атомите, образуващи същото единична ковалентна връзка, тогава истинските заряди на атома в молекулата също са идентични, тъй атоми образуват връзка еднакво опитен социализираното електронна двойка, такава връзка се нарича неполярен ковалентна връзка. Ако атомите са различни, тогава степента на собственост на социализирани двойка електрони се определя от разликата в electronegativities атоми, атома, с по-голяма Електроотрицателност все има двойка електрони, и следователно истински заряда е отрицателна, атом, с по-малко Електроотрицателност придобива съответно същата величина заряд, но с положителен знак.
2. облигации донор-акцептор. За образуването на този вид ковалентна връзка, както електрони има един от атомите (донор), втората от атоми, които участват в образуването на връзка се нарича акцептор. Получената молекула е официалната заряд на донор атом, се увеличава, и формалната заряд на акцепторен атом декрементирани.
3. полу-полярен връзка. Този вид ковалентна връзка е образувана между атом, имащ неразделен двойка електрони (азот. Фосфор. Сяра. Халогена и т. П.) И атом с два несдвоени електрони (кислород. Сяра). образуване на полу-полярен връзка се появява в два етапа:
1. Окисление (прехвърляне на един електрон) атом с NEP атом с два несдвоени електрони. В резултат на това атома с NEP превръща в радикал катион (положително заредени частици с несдвоен електрон) и атом с два несдвоени електрони - радикал анион (отрицателно заредени частици с несдвоен електрон).
2. социализация на несдвоени електрони (както в случая на проста ковалентна връзка).
При образуването на атом със семиполярна връзка NEP увеличава официално един дял и атом с два несдвоени електрони намалява тяхната официална един дял. механизми Flash-клипове химически връзки могат да се видят тук
Sigma (σ) -, пи (π) -връзките - приблизително описание на видовете ковалентни връзки в органични молекули, σ-връзка се характеризира с това, че плътността на електронен облак е максимална по оста, свързваща ядрата на атомите. При образуването на π -връзките извършва така наречената страна припокриване на електрони облаци, и плътността на електронен облак е максимална "горе" и "долу" равнината σ-връзка. Например, да етилен. ацетилен и бензол.
етилен С2 Н4 молекулата има двойна връзка, СН2 = СН2. електронния му формула: H: C :: С: H. Сърцевини етилен атоми са копланарни. Три електронни облаци от всеки въглероден атом образуване три ковалентни връзки с други атоми в една и съща равнина (с ъгъл между тях около 120 °). Cloud четвъртия въглероден атом на валентност електрон разположен над и под равнината на молекулата. Тези електронни облаци двата въглеродни атоми частично се припокриват над и под равнината на молекулата, образува втора връзка между въглеродните атоми. Първо, по-силна ковалентна връзка между въглеродните атоми, се нарича σ-връзка; втора, по-малко силен ковалентна връзка се нарича π-връзка.
Линейната молекулата на ацетилен
Е а-връзки между въглеродните атоми и водород, един σ-връзка между двата въглеродни атома и две π -връзките между въглеродните атоми. Две π -връзките намира над обхвата на а-връзки в две взаимно перпендикулярни равнини.
Всички шест въглеродни атома бензен циклична молекула С6 H6 лежат в една равнина. Между въглеродните атоми в равнината на пръстена са σ-връзка; същото комуникация при всеки въглероден атом, с водородни атоми. При изпълнението на тези връзки въглеродни атоми прекарват три електрон. Облаци четвърта валентност електрони на въглеродните атоми, имащи форма осмиците разположени перпендикулярно на равнината на молекулата на бензен. Всеки такъв облак припокрива с електронните облаци същите съседни въглеродни атоми. Молекулата на бензен не са оформени три отделни π -връзките и един π е електрон система на шест електроните, общи за всички въглеродни атоми. Връзка между въглеродните атоми в молекулата на бензен напълно идентични.
Връзката на ковалентна образуван чрез обмен на електрони (за образуване на общи електронни двойки), които се случват по време на припокриване на електрони облаци. При образуването на ковалентна връзка, включваща електронните облаци двата атома. Има два основни вида ковалентна връзка:
- Връзката на ковалентна се образува между неполярни неметални атоми на същия химичен елемент. Тези съобщения са прости вещества. например О2; N2; C12.
- Полярен ковалентна връзка е образувана между атоми на различни неметали.
В случай, например със солна киселина. общата плътност на електрони е изместен към страната на хлор, като хлорен атом настъпва частично отрицателен заряд. водороден атом - частичен положителен.
Примери за вещества с ковалентна връзка
Една проста ковалентна връзка свързан атома в молекули на прости газове (Н2. Cl2 и др.) И съединения (Н2 О, NH3. СН4. СО2. HCl и др.). Съединения с донор-акцептор връзка - амониев катион NH4 +. тетрафлуороборат анион BF4 - и други съединения с семиполярна връзка -. азотен оксид N2 О, О - -PCl3 +.
Кристали ковалентна изолатори или полупроводници. Типични примери на атомните кристали (атоми, които са свързани помежду си чрез ковалентни (атомни връзки)) могат да служат като диамант. германий и силиций.
Вижте какво е "ковалентна химична връзка" в други речници:
ХИМИЧНИ комуникации - връзката между атоми в молекулата или Mol. съединение резултат от прехвърляне или електронна поща, от един атом на друг нов д социализация двойка (или група) атоми. Силите водещ до X. с. Кулон, но X. с. описано от гледна точка на ... Физическо енциклопедия
ХИМИЧНИ комуникации - атома взаимодействие, в която електроните, принадлежащи към две различни атоми (групи) са чести (социализираното) за двата атома (групи), което води до свързване им до молекули и кристали. Има два основни типа Х. в. йон ... ... Най-Polytechnique енциклопедия
ХИМИЧНИ КОМУНИКАЦИИ - ХИМИЧНИ КОМУНИКАЦИИ, механизмът, чрез който атоми са свързани за образуване на молекула. Съществуват няколко вида на такава връзка, или на базата на привличане на противоположни заряди, или върху формирането на стабилни конфигурации чрез споделяне на електрони. ... ... Научно-техническа енциклопедия
Химическа връзка - връзка, взаимодействие на атоми, които прави техните съставни молекули и кристали. Работа с химически свързващи сили са предимно електрически характер. образуването на химична връзка е придружена от преструктуриране на ... ... Illustrated тълковен речник
Химическа връзка - взаимно привличане атоми, което води до образуването на молекули и кристали. Ние казваме, че молекула или кристал съществува между съседни атоми H. стр. Valence на атома (това, което подробно по-долу) показва броя на връзките ... The Great съветска енциклопедия
химична връзка - [химична връзка (свързване)] взаимно привличане атоми, което води до образуването на молекули и кристали. Валентността на атома показва броя на връзки, образувани с съседен данни атом. Терминът "химична структура" е въведена Академик А. М. Butlerov в ... ... Енциклопедичен речник на металургия
Йонната химичната връзка - йонна връзка силна химическа връзка, образувана между атоми с голям Електроотрицателност разлика, при който общото електронна двойка е напълно прехвърлени към атом с голяма Електроотрицателност. Пример за това е съединение на КЧС ... Wikipedia
Chemical Communications - химическо взаимодействие връзка атоми явление, причинено от натрупване на електрони облаци свързващи частици се придружава от намаляване на общата енергия система. Терминът "химична структура" първо се въвежда A. М. Butlerov през 1861 ... ... Wikipedia
Съобщение (химия) - взаимодействие Химическа връзка атоми явление, причинено от натрупване на електрони облаци свързващи частици се придружава от намаляване на общата енергия система. Терминът "химична структура" първо се въвежда A. М. Butlerov през 1861 ... ... Wikipedia