ковалентна връзка
Методът на валентните връзки, са следните:
1. връзка Ковалентното се формира от два електрона с противоположни завъртания, където електронната двойка принадлежи към два атома.
2. връзката на ковалентна е най-силни, толкова по-припокриващите електронни облаците.
Ковалентна връзка - вид химическа връзка. осъществявана чрез образуването на електронна двойка, която принадлежи към двата атома. Определен като ":" или "-".
На механизма на образуване на ковалентна връзка е разделена на:
- обмен ковалентна връзка;
- донор-акцептор ковалентна връзка.
Exchange ковалентна връзка възниква между въглеродните атоми. Когато всеки атом дава един несдвоен електрон в общата електронна двойка.
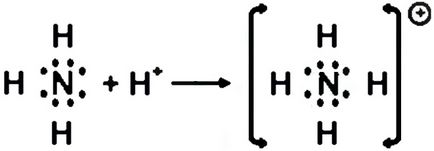
Донор-акцептор е ковалентна връзка, че един атом (донор) дава електронна двойка, а другата атом (акцептор) предвижда за тази двойка свободен орбитален.
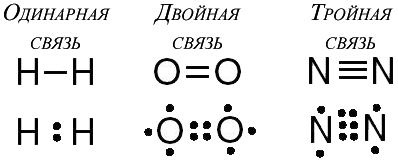
В допълнение към единични връзки, могат да образуват двойни и тройни ковалентна връзка.
Свойства на ковалентната връзка.
- насищане;
- ориентация;
- поляризуемост.
Saturation - способността да формират строго определена сума на ковалентни връзки (1 до 6), който определя максималната възможна валентност елемент.
Насоченост - аспирация атоми да образуват най-голямата електронна плътност между ядрата.
В поляризуемост - изместване на електрони под действието на външно електрично поле.
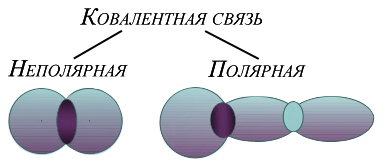
- неполярен ковалентна връзка, която е електронен облак, образуван от общата двойка електрони, разпределени в пространството симетрично по отношение на ядрата на двата атома (примери: Cl2, N2).
- полярен ковалентна връзка т.е. общата електронен облак smesh към един от атомите, така че има асиметрия в разпределението на заряда (примери: CO, H2O).
Електроотрицателност - е способността да се забави атомите, към себе си общо електронна двойка.