Двувалентни алкохоли (гликоли) - studopediya
Диоли съдържат в състава си две хидроксилни групи. Гликоли обща формула Cn H2N (ОН) 2.
Чрез систематични имена номенклатура диоли образувани от имената на затварянето с добавянето на алкани "диол" позиция показана на Фигури -ОН групи
Според един рационален номенклатура запазва името на съответните алкени с добавянето на думата "гликол"
Методите за получаване на гликоли. На двувалентни алкохоли могат да бъдат получени по същите методи като на едновалентни алкохоли или други. Най-важният от тях - по-долу:
1. Хидролиза digalogenoproizvodnyh:
2. Gipohlorirovanie алкени:
3. Хидролиза на етиленоксид:
4. окисляването на алкени.
Химически свойства. Поради взаимното влияние на мобилността на водородните атоми в хидроксилните групи на етилен гликол значително по-големи, отколкото в алкохоли. Гликоли имат големи киселинни свойства от алкохоли и взаимодействат не само с активните метали, но също и с метални хидроксиди, obrazuyuya сложни структури.
1. Взаимодействие с Cu (OH) 2 (качествен отговор гликоли):
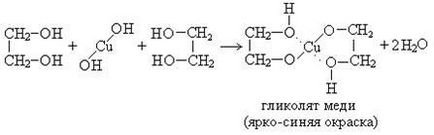
2. Взаимодействие с алкохоли:
По този начин образуването на моно- и diproizvodnyh.
3. междумолекулните дехидратация гликол:
4. Взаимодействие с минерални киселини:
Азотен естери притежават експлозивни свойства.
5. Gidrogalogenirovanie етиленгликол:
Заявление. Етилен гликол - вискозна безцветна течност, значително намалява точката на замръзване на водата и поради това се използва като антифриз, 60% етилен гликол воден разтвор замразява при -50 ° С Етилен гликол се използва в органичния синтез за получаване на полиестери, смоли, влакна LovSAN.
Тя се използва и при производството на печатарски мастила, печат върху плат.